يعتبر العلاج المناعي للسرطان من أكثر التطورات الطبية إثارة في السنوات الأخيرة، ولكن لماذا يفشل في كثير من الأحيان؟
السبب الخفي لفشل العلاج المناعي للسرطان في كثير من الأحيان
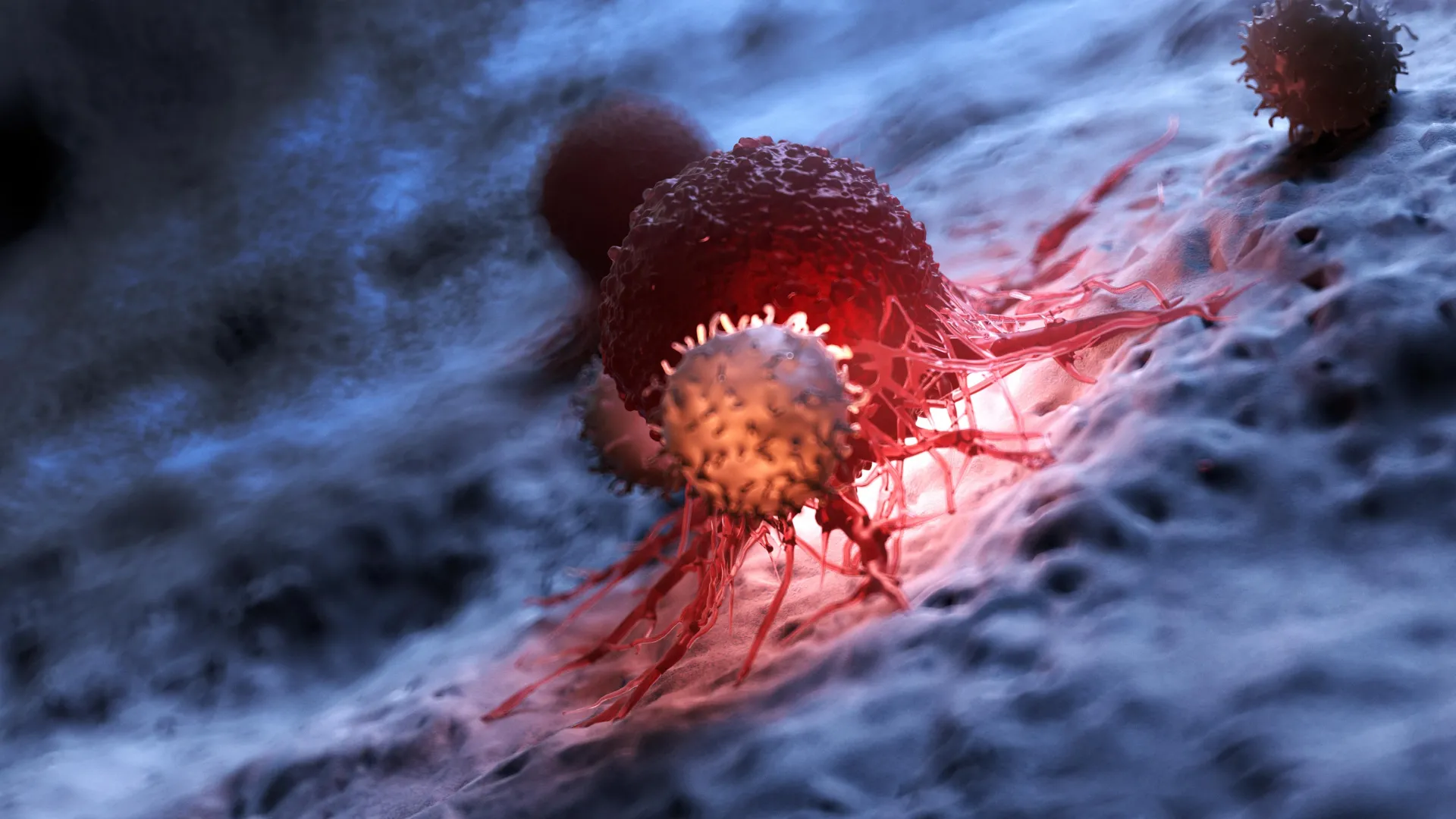
أعاد العلاج المناعي للسرطان تشكيل علاج السرطان عن طريق تدريب جهاز المناعة في الجسم على التعرف على الأورام ومهاجمتها. أدت الأدوية المعروفة باسم مثبطات نقطة التفتيش المناعية، والتي تستهدف مسار PD-1/PD-L1، إلى استجابات طويلة الأمد لدى بعض المرضى وزادت من التفاؤل بشأن السيطرة الدائمة على السرطان. ومع ذلك، بالنسبة لمعظم الناس، لا تقدم هذه العلاجات نفس الفائدة. يمكن للأورام أن تتكيف وتطور طرقًا للهروب من الكشف المناعي، مما يحد من فعالية العلاج.
تحديات جديدة في العلاج المناعي
وقد دفع هذا التحدي الباحثين إلى النظر إلى ما هو أبعد من الورم نفسه وفحص آليات أوسع للمقاومة المناعية. ويركز العلماء بشكل متزايد على كيفية تثبيط السرطان للنشاط المناعي في جميع أنحاء الجسم، وليس فقط في موقع الورم. تتضمن إحدى مجالات الاهتمام الناشئة الحويصلات الصغيرة خارج الخلية (sEVs)، وهي جزيئات صغيرة تطلقها الخلايا السرطانية يمكنها حمل جزيئات مثبطة للمناعة وإضعاف الاستجابة المناعية بطرق لا تزال غير مفهومة بالكامل.
التحقيق في كيفية تعبئة PD-L1 وإطلاقه
ولفهم هذه العملية بشكل أفضل، عمل فريق بحث من جامعة فوجيتا الصحية في اليابان، بقيادة البروفيسور كونيهيرو تسوتشيدا، مع متعاونين من مستشفى جامعة طوكيو الطبية وجامعة طوكيو الطبية. كان هدفهم هو الكشف عن كيفية تحميل PD-L1، وهو بروتين نقطة تفتيش مناعي رئيسي، بشكل انتقائي في sEVs وتحديد ما إذا كان من الممكن استهداف هذا المسار علاجيًا.
الدراسة التي نشرت في التقارير العلمية، تم بناؤها حول سؤال مركزي لم تتم الإجابة عليه. “تُطلق الخلايا السرطانية حويصلات صغيرة خارج الخلية تحتوي على PD-L1، والتي يُعتقد أنها تقلل من فعالية العلاج المناعي للسرطان. ومع ذلك، ظلت كيفية فرز PD-L1 في هذه الحويصلات غير واضحة.” أصبحت معالجة هذا اللغز هي أساس البحث.
لاعب جزيئي جديد في المقاومة المناعية
باستخدام مجموعة واسعة من التقنيات، بما في ذلك البيولوجيا الجزيئية والخلوية، والاختبارات الكيميائية الحيوية والدوائية، والعينات المشتقة من المريض، والمعلوماتية الحيوية، حدد الباحثون يوبيكويتين 3 (UBL3) كعامل رئيسي يتحكم في كيفية توجيه PD-L1 إلى sEVs.
ووجدوا أن PD-L1 يخضع لتعديل ما بعد الترجمة لم يكن معروفًا من قبل والذي يتضمن UBL3. يحدث هذا التعديل من خلال رابطة ثاني كبريتيد ويختلف عن العملية الكلاسيكية للتواجد في كل مكان. وأظهرت تجارب أخرى أن حمضًا أمينيًا محددًا، السيستين 272 في المنطقة السيتوبلازمية لـ PD-L1، ضروري لهذا التعديل.
عندما تمت زيادة مستويات UBL3 في الخلايا السرطانية، ارتفعت كمية PD-L1 المعبأة في sEVs بشكل حاد، على الرغم من أن إجمالي PD-L1 داخل الخلايا ظل دون تغيير. في المقابل، أدى انخفاض مستويات UBL3 إلى انخفاض واضح في تحميل PD-L1 في الحويصلات وإطلاقه خارج الخلية. وأكدت هذه النتائج معًا أن UBL3 يلعب دورًا مركزيًا في توجيه PD-L1 إلى السيارات الكهربائية الصغيرة.
تتداخل الستاتينات مع مسار الهروب المناعي الرئيسي
إحدى النتائج الأكثر إثارة للدهشة جاءت عندما قام الفريق بفحص الأدوية التي قد تتداخل مع هذه العملية. واكتشفوا أن الستاتينات، التي توصف على نطاق واسع لخفض نسبة الكوليسترول، تمنع بشدة تعديل UBL3. جميع الستاتينات المستخدمة سريريًا والتي تم اختبارها في الدراسة قللت من نشاط UBL3، وخفضت تعديل PD-L1، وانخفضت بشكل حاد كمية PD-L1 المصنفة في sEVs.
حدثت هذه التأثيرات بتركيزات دوائية منخفضة جدًا يمكن تحقيقها لدى المرضى ولم تكن مرتبطة بتأثيرات سامة على الخلايا. والأهم من ذلك، أن عينات الدم المأخوذة من الأشخاص المصابين بسرطان الرئة ذو الخلايا غير الصغيرة أظهرت نمطًا مشابهًا. من بين المرضى الذين يعانون من ارتفاع تعبير PD-L1 للورم، كان لدى أولئك الذين يتناولون الستاتينات مستويات أقل بكثير من sEVs المحتوية على PD-L1 في دمائهم مقارنة بالمرضى الذين لا يستخدمون الستاتينات.
اقرأ أيضًا...
وكشف المزيد من تحليل المعلومات الحيوية أن التعبير المشترك لـ UBL3 وPD-L1 كان مرتبطًا بنتائج البقاء على قيد الحياة لدى مرضى سرطان الرئة. يسلط هذا الاكتشاف الضوء على الأهمية السريرية المحتملة لهذا المسار التنظيمي المحدد حديثًا.
ماذا يعني هذا لعلاج السرطان
تساعد هذه النتائج مجتمعة في تفسير سبب فشل مثبطات نقاط التفتيش المناعية في كثير من الأحيان، وتشير إلى طريقة عملية لتحسين أدائها. تكشف الدراسة عن آلية خفية تنشر من خلالها الخلايا السرطانية PD-L1 المثبط للمناعة من خلال الحويصلات خارج الخلية، مما يسمح للأورام بإضعاف الاستجابات المناعية خارج بيئتها المباشرة.
يعد ربط هذا المسار بالستاتينات أمرًا مهمًا بشكل خاص لأن هذه الأدوية تستخدم على نطاق واسع وغير مكلفة وآمنة بشكل عام. وهذا يثير احتمال ترجمة النتائج إلى ممارسة سريرية بسرعة نسبية. وكما لاحظ الباحثون، “على المدى الطويل، قد يؤدي هذا البحث إلى علاجات مناعية للسرطان أكثر فعالية ويمكن الوصول إليها. ويمكن أن يساعد المزيد من المرضى على الاستفادة من علاجات نقاط التفتيش المناعية، وتحسين البقاء على قيد الحياة ونوعية الحياة في بيئات العالم الحقيقي.”
هدف جديد للتغلب على مقاومة العلاج المناعي
باختصار، تظهر الدراسة أن التعديل المعتمد على UBL3 يعزز تعبئة PD-L1 في sEVs وأن الستاتينات يمكن أن تعطل هذه العملية، مما يقلل من مستويات PD-L1 المثبطة للمناعة. ومن خلال تحديد حركة PD-L1 المرتبطة بالحويصلات كمحرك قابل للتعديل للهروب المناعي، يفتح البحث طريقًا جديدًا واعدًا لمعالجة مقاومة العلاج المناعي للسرطان. إن إضافة الستاتينات إلى استراتيجيات العلاج المركبة يمكن أن يوفر طريقة بسيطة وقابلة للتطوير لتحسين النتائج للمرضى الذين يتلقون مثبطات نقاط التفتيش المناعية.
المصدر :- Health & Medicine News — ScienceDaily
مع استمرار الأبحاث، يمكن أن تفتح هذه الاكتشافات آفاقًا جديدة لعلاج السرطان وتحسين جودة حياة المرضى.