في دراسة رائدة، تمكن الباحثون من تصور كيفية تدمير الخلايا التائية القاتلة للسرطان باستخدام تقنية الفحص المجهري المتقدمة.
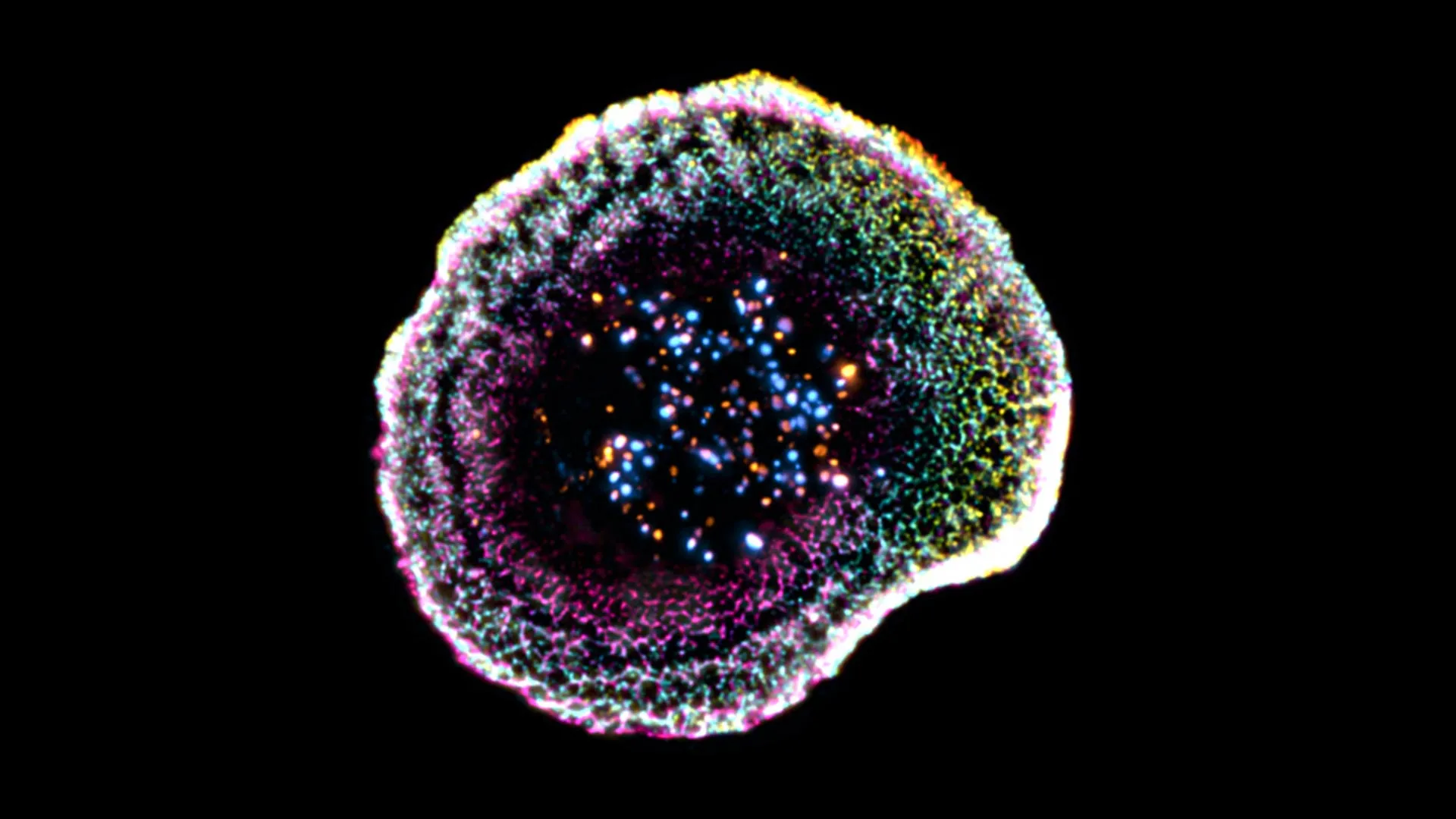
عرض ثلاثي الأبعاد يكشف كيفية تدمير الخلايا التائية القاتلة للسرطان
تعمل الخلايا الليمفاوية التائية السامة للخلايا كخلايا “قاتلة” متخصصة في الجهاز المناعي، حيث تبحث عن الخلايا المصابة أو السرطانية وتقضي عليها بدقة ملحوظة. تعتمد فعاليتها على نقطة اتصال يتم التحكم فيها بإحكام تسمى “المشبك المناعي”، حيث تطلق جزيئات سامة تدمر الهدف بينما تترك الخلايا السليمة المحيطة دون أن تصاب بأذى. وحتى وقت قريب، ناضل العلماء لمراقبة البنية الدقيقة لهذه العملية بالتفصيل. الآن، تمكن باحثون من جامعة جنيف (UNIGE) ومستشفى جامعة لوزان (CHUV) من تصور هذه الآليات في ثلاثة أبعاد في ظل ظروف شبه طبيعية. النتائج التي توصلوا إليها، نشرت في تقارير الخلية، سلطت ضوءًا جديدًا على كيفية دعم التنظيم الداخلي للخلايا التائية السامة للخلايا لوظيفتها ويمكن أن يؤدي إلى تقدم الأبحاث في علم الأورام المناعي.
آلية عمل الخلايا التائية القاتلة
عندما يواجه الجسم عدوى أو سرطانًا، ترتبط الخلايا الليمفاوية التائية السامة للخلايا بإحكام بهدفها وتشكل المشبك المناعي. ومن خلال هذه الواجهة المتخصصة، فإنها تطلق مواد سامة تؤدي إلى تدمير الخلية الضارة. يسمح هذا النهج المستهدف لجهاز المناعة بإزالة التهديدات بكفاءة مع تقليل الأضرار الجانبية للأنسجة القريبة.
التحديات في دراسة البنية الخلوية
وعلى الرغم من أن العلماء قد فهموا منذ فترة طويلة أساسيات هذه العملية، إلا أن دراسة بنيتها التفصيلية على مقياس نانومتر داخل الخلايا البشرية السليمة ظلت صعبة. وتتمثل إحدى الصعوبات الرئيسية في كيفية إعداد العينات، حيث أن الطرق التقليدية يمكن أن تشوه المكونات الخلوية الحساسة. غالبًا ما تجبر تقنيات التصوير الحالية الباحثين على الاختيار بين الدقة العالية، أو مجال رؤية واسع، أو الحفاظ على البنية الطبيعية للخلية.
تقنية الفحص المجهري المتقدم
للتغلب على هذه التحديات، استخدم فريق UNIGE وCHUV-UNIL، بدعم من برنامج ISREC Foundation TANDEM، طريقة متقدمة تسمى الفحص المجهري للتوسع بالتبريد (cryo-ExM). “تتضمن هذه التقنية تجميد الخلايا بشكل فوري بسرعة عالية جدًا، ووضعها في ما يسمى بالحالة الزجاجية، حيث يتصلب الماء دون تكوين بلورات وبالتالي يحافظ على الهياكل البيولوجية بأمانة. ثم يتم توسيع العينات فعليًا باستخدام هيدروجيل ماص، مما يجعل من الممكن مراقبة تنظيمها الداخلي بدقة كبيرة مع الحفاظ على بنيتها شبه الأصلية،” تشرح فيرجيني هامل، محاضرة أولى في قسم البيولوجيا الجزيئية والخلوية في كلية العلوم بجامعة UNIGE.
الكشف عن سمات هيكلية جديدة
وباستخدام هذا النهج، كشف الباحثون عن سمات هيكلية جديدة عند النقطة التي تصل فيها الخلية المناعية إلى هدفها. “يكشف عملنا أنه عند نقطة الاتصال بين الخلية المناعية وهدفها، يشكل الغشاء نوعًا من القبة، التي يبدو أن بنيتها مرتبطة بتفاعلات الالتصاق وبالتنظيم الداخلي للخلية”، كما يشير فلوران لوميتر، باحث ما بعد الدكتوراه في قسم البيولوجيا الجزيئية والخلوية في كلية العلوم بجامعة UNIGE والمؤلف الأول للدراسة. كما قام الفريق بفحص الحبيبات السامة للخلايا، المسؤولة عن قتل الخلايا المستهدفة، بوضوح غير مسبوق. ووجدوا أن هذه الحبيبات يمكن أن تختلف في البنية، حيث تحتوي في بعض الأحيان على “قلب” واحد أو أكثر حيث تتركز الجزيئات النشطة.
توسيع البحث إلى الأورام البشرية
ووسع الباحثون طريقتهم إلى ما هو أبعد من الخلايا المعزولة، وطبقوها مباشرة على عينات الأورام البشرية. “لقد قمنا بتوسيع هذا النهج ليشمل أنسجة الورم البشرية، مما يجعل من الممكن مراقبة الخلايا الليمفاوية التائية المتسللة للأورام بشكل مباشر وآلياتها السامة للخلايا على مقياس النانومتر. وهذا يسمح لنا بدراسة الاستجابات المناعية مباشرة في سياقها السريري وفهم الآليات التي تحدد فعاليتها بشكل أفضل،” تشرح بينيتا وولف، رئيسة المقيمين والباحثين المساعدين في قسم علم الأورام السريري في جامعة CHUV، والتي شاركت في قيادة الدراسة.
اقرأ أيضًا...
إطار عمل لدراسة الاستجابات المناعية
ومن خلال تقديم رؤية ثلاثية الأبعاد وشبه أصلية لكيفية عمل هذه الخلايا المناعية، يقدم هذا العمل إطارًا قيمًا لدراسة الاستجابات المناعية في ظروف العالم الحقيقي. يمكن أن تساعد هذه الأفكار في تحسين العلاجات، خاصة في علم الأورام المناعي، من خلال تحسين فهمنا لما يدفع الهجمات المناعية الناجحة ضد السرطان وما يحد منها.
المصدر :- Health & Medicine News — ScienceDaily
تقدم هذه النتائج رؤى جديدة قد تعزز من فعالية العلاجات المناعية وتساعد في مكافحة السرطان بشكل أفضل.